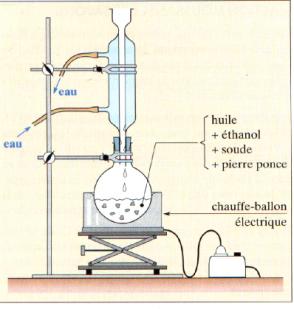
Chauffage à reflux

Filtration sur filtre Büchner
|
TP Chimie N° 12 |
Fabrication d'un savon de Marseille : Correction |
IV- Exploitation.
1)-
Faire les schémas annotés des différentes étapes.
|
Chauffage à reflux |
Filtration sur filtre Büchner |
2)-
Quel est le type de montage utilisé lors de l'expérience 1 ? Quels sont les
rôles du montage utilisé ?
- On utilise le chauffage à reflux. En chauffant, on augmente la température du mélange réactionnel, on accélère la réaction de saponification qui est une réaction lente à température ambiante. Le chauffage à reflux permet de condenser les vapeurs des réactifs et des produits grâce au réfrigérant à bulles et de les faire retourner à l'état liquide dans le ballon.
3)-
Pourquoi agite-t-on le mélange réactionnel au cours de l’expérience ?
Quel est le rôle de l'éthanol ?
- Le corps gras et la solution de soude ne sont pas miscibles, on agite pendant l'expérience pour maintenir les réactifs en contact.
- L'utilisation de l'éthanol rend le mélange réactionnel plus homogène.
4)- Indiquer
les observations lors de l’expérience 2. Quel est le but du relargage ?
Pourquoi effectue-t-on le relargage avec une solution aqueuse saturée de
chlorure de sodium ?
- L’expérience 2 est le relargage. Lorsque l’on verse le mélange réactionnel, dans la solution aqueuse glacée de chlorure de sodium, le savon précipite.
- Le relargage permet de récupérer le savon.
- La présence des ions chlorure et des ions sodium diminue la solubilité du savon et facilite la précipitation.
5)-
Qu’est-ce qu’un acide gras ? Écrire la formule semi-développée de
l'acide oléique en mettant en évidence la double liaison.
- Un acide gras est un acide carboxylique à chaîne linéaire, saturée ou non, possédant en général un nombre pair d'atomes de carbone, entre 4 et 22.
- L’acide oléique est un acide gras : acide (Z) octadéc-9-énoïque. Il possède 18 atomes de carbone et une double liaison. C’est un acide gras insaturé.
- Formule semi-développée :
|
|
|
|
6)-
Qu’est-ce qu ‘un corps gras ? Comment obtient-on un corps gras ?
écrire la réaction chimique de
la formation d’un corps gras.
- Un corps gras est un triester d'acide gras et du glycérol. Les corps gras sont encore appelés triglycérides.
- Il s’agit d’une réaction d’estérification entre des acides gras et un alcool, le glycérol.
- Le glycérol est un trialcool : le propan-1, 2,3 - triol.
|
|
|
- Équation chimique : estérification.
|
|
7)- Écrire
la formule semi-développée de l'oléine.
- Formule semi-développée de l’oléine :
|
|
8)- Écrire
l'équation de la réaction de saponification de l'oléine.
- Réaction de saponification de l’oléine :
|
|
9)- Déterminer
la quantité de matière n 1
d'ions hydroxyde introduits dans le milieu réactionnel. Déterminer la
quantité de matière n 2
d'oléine introduite dans le milieu réactionnel. Quel est le réactif en excès
?
- Quantité de matière d’ions hydroxyde introduits.
- Quantité de matière d'ions hydroxyde :
-
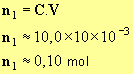
- Quantité de matière d'oléine :
-
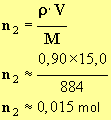
- L’ion hydroxyde est le réactif en excès car
-
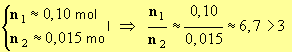
10)- Déterminer
la masse m de
savon sec que l'on peut espérer recueillir. Calculer le rendement de la réaction.
- Masse de savon sec que l’on peut espérer obtenir :
- Masse de savon : la soude est en excès, c'est l'oléine qui limite la réaction.
- Masse molaire de l'oléate de sodium : M(oléate de sodium) = 304 g / mol.
-
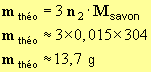
- On a obtenu la masse de savon suivante : m exp ≈ 10,2 g
- Rendement de la réaction :
-
